动物活体内细胞捕获和操控
在动物活体环境下研究单个细胞的结构和功能以及细胞与组织之间的相互作用可以帮助揭示细胞病变的机理、血栓形成机制和肿瘤细胞迁移特性等,对于生物医学基础研究和临床诊断具有重要意义。但长期以来生物医学科学家苦于没有合适的非损伤性操控细胞的技术手段。我们实验室首次将光镊技术应用于动物活体的研究取得突破,研制出适合于动物活体内细胞操控的活体光镊装置,并成功利用该装置实现小鼠耳朵血管内红细胞的操控以及对血管的可控阻塞和疏通[1]。本研究技术能直接深入到动物活体内对细胞进行实时观察、操控,实施非接触式手术的实验取证,从而开拓了光镊技术研究活体动物新领域,为活体研究和临床诊断提供了一种全新的技术手段。
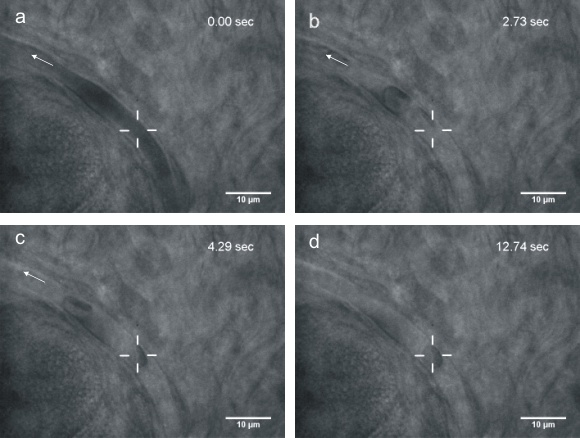
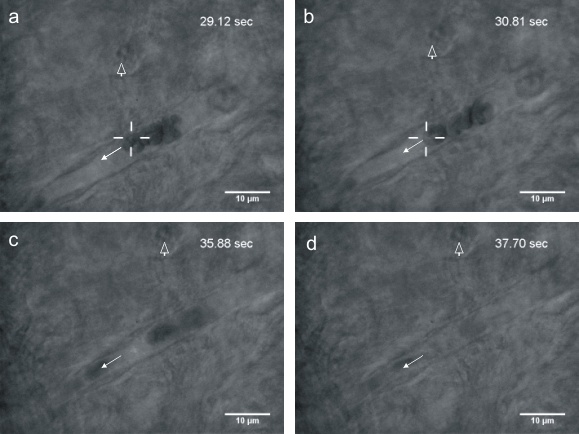
光镊研究rpoS RNA分子结构
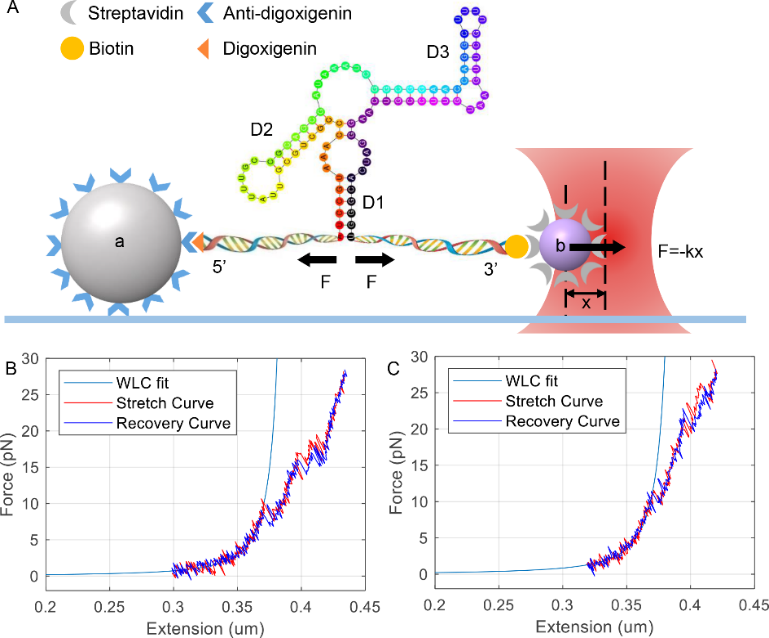
位于rpoS mRNA 5'UTR的自抑制茎环对细菌全局应激响应因子的表达具有重要的调控作用。因常规的晶体学和核磁共振均不适合研究RNA的空间结构,我们发展了一种通过光镊拉伸来考察RNA结构变化动态过程的方法。利用光镊测量出镁离子结合引起RNA局部结构结合的自由能变化,并以此推测镁离子导致了RNA结合更加紧密进而改变RNA stem loop的取向。实验发现rpoS拉伸曲线的精细结构有几种不同的打开方式,有一次性打开和多次分段打开的情况,且打开所需的力不尽相同,这些现象对应RpoS的几种不同的折叠方式。这一猜想被X射线散射实验和AFM所证实[2]。本研究对理解自抑制茎环空间结构及其生物学功能提供了支持。
光镊研究细胞膜的动力学行为
我们采用光镊从细胞上牵拉出膜丝是研究细胞膜机械性质。根据膜丝直径与张力的依赖关系,我们建立了描述光镊控制下膜丝张力弛豫过程的物理模型。用模型对每条弛豫曲线进行拟合,得到一系列等效粘滞系数和静态张力,通过膜丝的弛豫曲线研究细胞膜动力学特特性。实验上方法是利用光镊操控Lectin修饰的小球与细胞接触使之黏连,然后再离开。从细胞膜上拉出直径约为200nm的膜丝。当拉伸停止以后光镊测得的张力随时间逐渐下降。这一动态过程体现了细胞膜的流动性以及膜蛋白和骨架的物理性质[3]。


新型光镊技术
光镊作为一种高精度、无接触的光学微操控工具,被广泛用于捕获和操控生物细胞和微纳米颗粒,研究细胞的结构、功能和相互作用,在生物医学和光子学领域具有重要的应用价值。传统光镊技术依赖于紧聚焦的高斯激光束梯度力阱实现微粒的囚禁和操控。这种光阱也给细胞操控带来一些的局限性,例如高斯光阱操控功能单一,无法应对复杂操需求的应用场景;聚焦激光对生物细胞的热损伤较大;光梯度力作用范围小,无法操纵大量的生物细胞。为了应对这些挑战,一方面我们结合结构光场的特殊时空演化特性实现新型操控功能;另一方面,引入不同外场,如流场、电场、等离子场等,开发操控精确度更高、范围更大的操控技术。
在密集环境下如血管和淋巴结内操控单个细胞会受到周围环境的影响。为此,我们提出一种环形的光阱,利用其作为光学围栏,为目标细胞的捕获和操控建立一个安全区域。利用该方案,我们实现了在密集环境下单个血细胞的捕获和操控。此外,我们还将研究拓展至淋巴结内免疫细胞的操控。淋巴结内免疫细胞是集中在一起的,挤压出的淋巴细胞处于密集环境,为了对单个细胞进行操控和研究细胞间相互作用。我们构建了光学围栏下的双光阱,实现了两个细胞的独立操控和碰触操作[4]。


光热损伤是细胞光捕获不可避免的一个效应。传统聚焦激光光束在焦点附近的功率密度很高,这个光热损伤效应尤其明显。为了减小光捕获对细胞的损伤,我们提出一种新型结构光场光镊,采用角向偏振矢量光束作为捕获光。角向偏振光束在紧聚焦条件下,其光束中心是暗场分布,且具有更好紧聚焦特性。这使得它能够提高轴向的捕获效率,并有效降低光热损伤效应。我们利用该光镊在斑马鱼活体内进行了血细胞的捕获实验,研究结果表明相同入射功率下,角向偏振光镊能够提供更安全的捕获效果[5]。

我们与张斗国教授合作提出了一种基于一维光子晶体薄膜的光流体细胞操控新方法[6]。该方法采用一维光子晶体,其负载的布洛赫表面波模式具有局域电场增强特性。由于多层膜的固有光损耗(特别是其中的氮化硅膜层),聚焦光能转换成局域热能,形成稳定分布的温度梯度场。介质薄膜由于导热性低于金属薄膜,可以形成更高的温度梯度,这有利于实现低功率的热泳操控。基于上述全介质光子晶体的光流体效应,在光热耦合场中的长程热对流力、局部热泳力、短程光梯度力的共同作用下,单细胞捕获和操控、大量酵母细胞和大肠杆菌细胞的可逆自组装得以实现。该方法同时兼顾了传统光镊和热泳操控的优点,能够将细胞快速远程运输到聚焦光场附件,实现单个细胞的稳定捕获后进行大量细胞的聚集组装,为生物细胞的远程传输、分类、自组装和群体感应的研究提供了一种新手段。
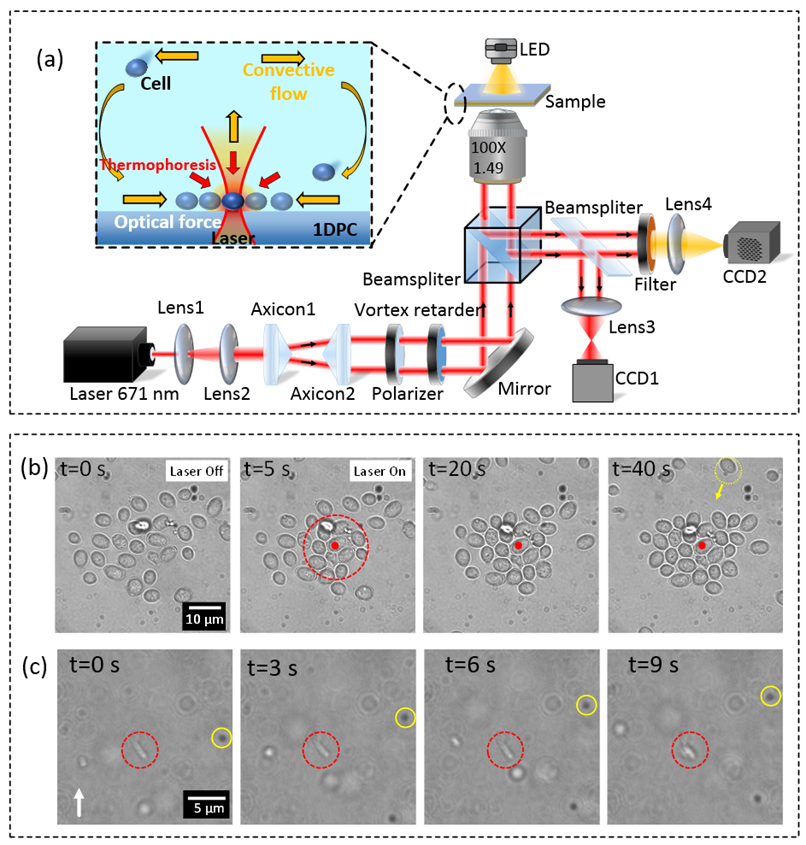
拉曼光镊光谱(研制中)
光镊与拉曼光谱结合被称为拉曼光镊技术。拉曼光镊被广泛应用于生物医学研究中,因其具有微量检测、快速和高精度等优点,特别适合生物样品的化学成分分析。我们课题组目前正在研制适用于生物纳米颗粒(外泌体)检测的拉曼光镊,采用光热镊、光电镊、电热等离子镊等技术克服传统聚焦光镊对于生物微粒的活性应用。应用方面,我们课题组和第一附属医院开展合作研究,采用拉曼光谱研究肿瘤细胞和健康体细胞外泌体特性,载药囊泡的治疗效果,从新的角度探索肿瘤细胞免疫逃逸机制。
参考文献:
[1] Trapping red blood cells in living animals using optical tweezers. Nature Communications, 4, 1768 (2013).
[2] Conformation and mechanical property of rpoS mRNA inhibitory stem studied by optical tweezers and X-ray scattering. PLoS ONE 14(9): e0222938 (2019).
[3] Measurement of dynamic membrane mechanosensation using optical tweezers. Journal of Molecular Cell Biology, 2021, 13(6), 455–457.
[4] Trapping and Manipulation of Single Cells in Crowded Environments. Frontiers in Bioengineering and Biotechnology 8, 422 (2020).
[5] Reducing photodamage in optical trapping of individual cells in living zebrafish[J]. Applied Physics Express, 13(3): 032008 (2020).
[6] Controllable optofluidic assembly of biological cells using an all-dielectric one-dimensional photonic crystal. Photonics Research 10, 14 (2022).


